参考观研天下发布《2018年中国放射性药品市场分析报告-行业深度调研与发展前景预测》
放射性药品是由放射性同位素搭配专门定位于特定器官及组织的分子试剂组成。之后,试剂将放射性同位素输送至特定器官、组织或细胞。患者通过口服或注射服用放射性药品。核医学医师利用伽玛照相机(如PET或SPECT)检测用于特定疾病诊断及治疗的放射性药品所含放射性同位素发出的辐射。一、行业发展特点
我国核素药物应用始于20世纪50年代后期,1989年国务院颁布了《放射性药品管理办法》(2017年3月修订版发布),标志着我国核素药物研究、生产、经营、管理进入规范化时期,促进了核素药物的健康发展。根据全国核医学现状普查结果统计,截至2015年末我国从事核医学相关工作的科室891个,开展核素治疗的医疗机构658个,不到一半的三甲医院配备了SPECT/CT(不包括SPECT),而价格更为高昂的PET/CT的普及率更低(三甲医院渗透力不到1/3),整体来看我国核医学及核素药物市场仍有很大成长空间。
数据显示,近年来我国的核医学无论是在科室数量、从业人员数量、设备配置数量,还是在开展诊治的人次等方面均有不同程度的增长,呈现出良好的发展态势。此外,在新产品研发、国际合作、学术交流、人才队伍建设等领域也都取得了积极进展。面对看似乐观的行业发展形势,核医学界在备受鼓舞的同时但也不免有些担忧,因为快速发展是建立在此前相对薄弱的基础上的。
目前,国内外放药研发的差距主要在于:一是核素少,这就造成临床科研能使用到的原料品种少,研发受到限制。二是放药用量小,且集中于诊断,多为一次性使用。这导致了研发的收益小、投入大,打击了行业的积极性。三是新药申报流程长、难度大,导致科研单位积极性不高。另一方面,相比国外,我国从事放药研发的专业人才储备不足。
作为一种药物,放射性药物首先要符合国家监管部门对药物统一的监管标准和规范。但放药又是属于医疗用毒性药品、麻醉药品、精神药品、放射性药品等四种特药的监管范围,也要体现出和普通药物的不同,制定相应的具体政策。监管也要更加细化,更具可操作性。我国的《放射性药品管理办法》于1989年发布实施,至今已经有近30年的时间。放药行业也在呼吁国家监管部门,借鉴国际先进经验,推动《办法》的重新修订,实现更科学的监管,促进行业发展,也带动核医学的发展。
我国的放射性核素供应基本依赖进口,价格高且不能按时供给,严重制约我国放射性药物行业发展。运行中的反应堆归属不同的国营科研单位, 各自承担不同的国家科研任务,医用同位素的供应只是辅助任务,难以满足国内的需求。近年来,东诚药业集团子公司云克药业依托中国核动力研究设计院积极研究设计建造专用的医用同位素生产堆(MIPR),可同时生产99Mo、131I和89Sr2,对于解决我国医用核素供应紧张,掌握行业上游资源,具有积极意义。
二、行业市场规模
近年来,我国诊断用放射性药物的发展远快于治疗用放射性药物,其中诊断药物约占总量的80%,而治疗药物仅约占20%。随着国内核医学的进步及国家和公众对于放射性药物认识的不断提高,国内放射性药物产业发展较迅速,近些年销售收入以每年约25%的幅度增长。据研究报告,国内的放射性药物产业主要分布在成都、北京和上海,其中成都与北京产业规模相当,各占40%左右。2017年,我国放射性药品市场规模大约在36亿元,预计2018年将达到46亿元。
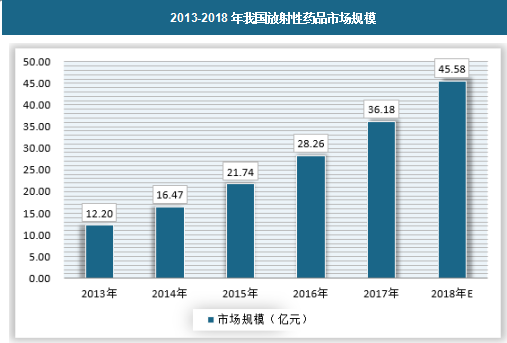
资料来源:观研天下数据中心整理
三、市场供需分析放射性药品的生产、流通、使用受到多个部门较为严栺的管理,具有较高的进入门槛,竞争有序。目前国内共有放射性药品企业约20家,其中中国同辐集团市场规模领先。
由于准入门槛较高,放射性药品从研发到生产、供应市场的周期比较长,一般都需要五年以上,有的甚至得十年、二十多年。放药新产品的注册要经历立项、研发、检测、动物实验、临床实验等严格、漫长的步骤,直至送到国家食药总局评审。
近年来,随着国内核医学的进步、国家和公众对于放射性药物的认识不断提高,国内放射性药物产业发展较迅速,销售收入以每年25%的幅度增长。
我国是个人口大国,同时,也是一个癌症大国,据国家癌症中心发布的2017年最新癌症数据来看,与2012年相比,中国癌症新发人数上升,从358万上升到368万,增幅3%, 2017年世界癌症新发病例为1409万,也就意味着中国新发癌症病例占世界的1/4。未来几年,随着人口老龄化的加重以及现代生活方式的转变,这一数字可能会更大。
从供需平衡来看,过去大量的非法获得放射性药品的现象表明市场需求是大于供给的,供不应求的现象难以缓解。
未来由于我国市场需求将会逐步放开,得益于行业的供给管制有所放松,加上分级医疗制度的不断完善和医疗保险覆盖面的扩大,以及我国目前仍就不断提高的老龄化比例和癌症患病率,未来市场的供不应求状态短期内仍旧难以改变。
四、发展趋势
1、核素生产
近年来,医用同位素用量的年增幅维持在10%左右[4],全球的核原料供应偏紧已成为放射性药物行业发展的瓶颈。加上我国供应医用同位素生产的反应堆匮乏,核素供应基本依赖进口,建立产能高、安全性好的医用同位素生产方法将有利于我国放射性药物行业的健康快速发展。为此,一是要积极建造专用的医用同位素反应堆MIPR,实现99Mo等核素的自主生产、规模供应,逐渐摆脱国内核原料供应紧张的问题;二是加快基于加速器的核素制备开发步伐,发展99mTc和89Zr、64Cu、211At、123I等多种具有良好应用前景的核素制备方法,减少对反应堆生产核素的依赖。这方面国内的研究机构和企业有一定的技术储备。北京大学肿瘤医院在国内率先制备了PET核素64Cu供研究之用,东诚安迪科也实现了PET核素89Zr的试生产,可供企业内部使用。
2、研发方向
从标记应用的核素方面看,伴随PET技术的发展以及正电子核素制备技术的日趋成熟,以18F、68Ga标记的诊断用放射性药物发展迅速,是当前诊断用放射性药物的研究热点,如靶向神经内分泌瘤的NETSPOT(68Ga-dotatate)、靶向阿兹海默病淀粉样蛋白18F-Florbetapir、靶向前列腺癌的18F-fluciclovine(anti-18F-FACBC)。治疗用放射性药物尽管目前应用于临床的品种很少,但因其具有很好的市场和经济效益,日益受到重视。近年来欧美陆续有治疗性放射性药物批准上市,如氯化镭[223Ra]注射液(商品名Xofigo)、177Lu-DOTATATE(商品名LUTATHERA),使得国内外对包括223Ra、177Lu、211At、225Ac等治疗性核素标记的放射性药物产生极大关注。177Lu的生产需要利用反应堆176Lu(n,γ)177Lu。已有研究表明α放射性核素靶向治疗具有非常好的临床潜力,211At和225Ac靶向治疗目前处于临床试验阶段。然而α放射性核素的生产在技术上有很大的挑战,供给十分匮乏。211At的生产可利用中等能量的加速器通过209Bi(α,2n)211At反应实现。
分子影像是精准医疗的三大核心技术之一。新的放射性药物开发朝着诊疗一体化方向发展:用诊断性放射性核素标记对疾病靶点具有高特异性和靶向性的分子(如单抗或多肽),对病人进行筛查诊断,确诊后再用治疗性核素标记的靶向性药物进行个体化治疗,将疾病的诊断和治疗充分联动起来,使医生的临床诊治更有针对性、准确性和规范化,真正实现个体化的疾病早期诊断和精准治疗,能够挽救更多癌症病人的生命。欧美现已获批的68Ga-DOTATATE和177Lu-DOTATATE即是当前诊疗一体化药物的典型。
3、法规政策
欧美针对放射性药物的特殊性,均有出台与之相匹配的注册申请文件、技术指导原则,且支持放射性药物在无IND(申请临床研究)批准下的早期临床开发活动。相比之下,我国缺乏系统性强的、与当下核医学技术进展匹配度高的、详实有效的放射性药物管理体系,近十几年来无一例放射性药品获批[12]。因而尽快全面修订《放射性药品管理办法》,同时完善相关的政策和指导原则,建立符合放射性药物特点的、管控有效的、与现行药物管理法规接轨的放射药物管理体系,使之满足和适应当今放射性药物发展的需要,将是我国放射性药物未来发展的重要任务。
4、人才队伍建设
放射性药物行业专业性强、人才储备较少,这是我国放射性药物创新速度慢的原因之一。因此我国应注重加强对放射性药物研制、生产、使用的专业人才培养。
在国家层面,应该鼓励和扶持放射性药物企业成为放射性药物开发和生产的主体,鼓励校企合作,凝聚一流人才,共同打造具有国际先进水平的研发中心。放射性药物企业也应针对重大疾病的精准诊疗,积极开发具有自主知识产权的创新放射性药物。企业和学校应通过协作建设技术人才培训基地,提高放射性药物从业人员的专业素质,为我国未来放射性药物诊疗一体化的爆发性发展提供强大动力。
5、专业平台建设
放射性药物的研制需要稳定的核素来源、完善的基础设施及专门的大型仪器等。目前国内的资源相对分散,不利于放射性药物的顺利发展。因此,整合行业核心研发资源,着力解决核素生产和供应问题,对放射性药物的开发具有重要的支撑作用,对推动我国放射性药物领域的科技进步和相关产业的发展具有重要意义。

【版权提示】观研报告网倡导尊重与保护知识产权。未经许可,任何人不得复制、转载、或以其他方式使用本网站的内容。如发现本站文章存在版权问题,烦请提供版权疑问、身份证明、版权证明、联系方式等发邮件至kf@chinabaogao.com,我们将及时沟通与处理。